2012年2月,一个合资企业正式诞生,由三星生物和百健(Biogen)成立的公司取名三星Bioepis。
如今,五年过去了,三星Bioepis开始将生物类似药卖到欧美。
“五年前,我们进入生物制药行业,决心通过创新替代传统流程,将治疗方法带给患者,“三星Bioepis首席执行官兼总裁Ko Han-sung 在一份声明中说。
三星旗下有两个生物制药公司,三星生物(Samsung Biologics)负责生物药的生产和外包,而三星Bioepis负责生物类似药。
八月底,三星接连不断传出消息让行业人士耳目一新。
周一,三星Bioepis宣布与武田制药(Takeda Pharmaecuticals)签约,共同开发新药,首先是武田的急性严重胰腺炎用药TAK-671.
双方将共同出资,分担风险。
目前,急性严重胰腺炎没有有效治疗方法,公司在声明中表示。
接着,周五,三星Bioepis再传消息,生物类似药Imraldi获得欧盟批准。这是世界级畅销生物大药,艾伯维的修美乐(Humira)的生物类似药。
在欧盟28个国家获批的适应症有9个,包括:牛皮癣,克罗恩病,类风湿关节炎,幼年特发性关节炎,轴向脊椎关节炎,银屑病关节炎,化脓性荨麻疹,溃疡性结肠炎和葡萄膜炎。
这是三星在欧盟获批的第三个抗肿瘤坏死因子(TNF)的生物类似药。去年,欧盟委员会批准了公司的Benepali(SB4),这是恩利(Enbrel), 依那西普的生物仿制药和Flixabi(SB2),类克(Remixade), 英夫利昔单抗的生物仿制药。
三星的Imraldi也是欧盟批准的第四个生物类似药。目前,三星有六个生物类似药产品,是韩国药企中拥有生物类似药管线最多的一家。
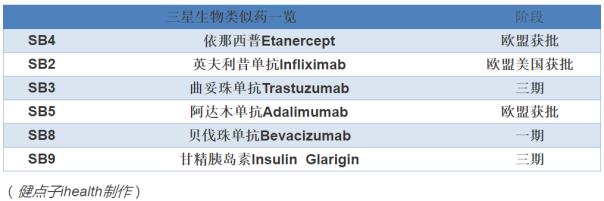
三星的生物类似药发展迅猛,原因何在呢?
其中一个原因,积极联姻。
三星Bioepis成立伊始,就和美国默克公司在2013年2月达成合作伙伴关系。
根据协议,三星Bioepis专注于临床前和临床开发,负责工艺开发和产品的临床试验和注册,而默沙东将负责商业化。
默沙东全面负责英夫利昔单抗在美国市场的商业化。
如今,最新的一项与武田的协议将促使三星向新药研发型企业转型。
此外,三星还积极准备到美国达斯达克上市,预计融资10亿美元。三星Bioepis的市值将达到约8万亿韩元(约67.6亿美元)。
